Липсата на протеини на регулаторите на комплемента система
Има случаи, неуспех
Съдържание
провала си Това удължава живота на C3b в състава С3 konvertaznogo комплекс (S3bBb) алтернативна пътека. В резултат на пътя остава постоянно активира и С3 са все разцепен за образуване C3b. Интравенозното инжектиране на плазма или пречистени фактор I увеличава бързо концентрация С3 в серума на пациента и нормализирана С3-зависима функция (по-специално, бактериални опсонизиране) ин витро.
Дефицит на фактор Н има същите клинични прояви са били фактор Н улеснява гниене С3 конвертаза път заместник. Във всички известни случаи, нивата на C3 и фактор В и общо хемолитична активност на комплемента и активността на неговата алтернатива път са силно намалени. Пациентите претърпели непрекъснато системни инфекции, причинени от бактерии, пиогенни особено менингококови и почти 50% се наблюдава гломерулонефрит. При някои пациенти с установено недостатъчност С4-свързващ протеин, неговото ниво е приблизително 25% от нормата.
Всички те специфични заболявания липсващ, въпреки че един пациент е имал ангиоедем и болест на Бехчет.
В недостатъчност на пропердин значително увеличава честотата на менингококов менингит. Това състояние се появява само при мъже, подчертава ролята на алтернативен път на активиране на комплемента в защитата на организма от бактериална инфекция. При пациенти със запазена нормална хемолитична активност на комплемента в присъствието на специфични антитела антибактериални необходимо за активиране на алтернативен път и пропердин е значително намалена. Случаи на кожен васкулит и дискоиден лупус еритематозус.

за С1 дефицит инхибитор наследствен характеризиращ ангиоедем. При пациенти на 85% от засегнатите семейства на концентрацията на инхибитор представляват само 5-30% от нормата, докато другите нива на този протеин (реакция със специфични антитела) са нормални или дори повишени, но протеин оказа функционално активна. И двете форми на заболяването са наследени по автозомно доминантен начин.
Видео: Системата на комплемента. МАК. имунология | Системата на комплемента. MAC. имунология
Без С1 инхибитор Активността на този компонент става неконтролируемо: засилено разпадане на С4 и С2, което води до образуването на вазоактивни пептиди (кининови). В резултат на тяхното действие върху съдоразширяващи посткапилярни ниво от време на време възникват на местно ниво "стегнат" подуването. С1 активиране механизъм при тези пациенти не е ясно.
оток Тя се разраства бързо и е придружена от обрив, сърбеж, промяна в цвета или хиперемия на засегнатите райони. Обикновено няма болка и въпреки подуване на чревната стена може да предизвика тежки коремни спазми, повръщане и диария понякога. Това не винаги е придружен от подуване на кожата, както и пациенти понякога се обръщат към хирург или психиатър. Оток на ларинкса може да доведе до смърт. Произтичащи от травми, физически и емоционален стрес, или по време на менструация, атаки продължиха в продължение на 2-3 дни, а след това постепенно отшумяват. Те може да се случи за първи път и до 2-годишна възраст, но стават особено тежка в големи деца или тийнейджъри.
В-лимфоцити тумор или автоантитела към C1 инхибитор може да бъде причина за придобита недостатъчност C1 инхибитор. Индивидите с наследствен дефицит своята наблюдавана SLE и гломерулонефрит.
C3b Той стимулира образуването на комплекс С3 BBB като С3 konvertaznoy активност. Образуването и стабилизиране на комплекса мембрана възпрепятства три допълнение регулаторен протеин: PK1, мембрана кофактор протеин и FSD S3bBb. CD59 (мембрана инхибитор на реактивен лизис) инхибира комплекс възел мембрана атака, образувайки "дупки" в целевата мембрана. При липса на FSD и CD59 по повърхността на червените кръвни клетки се развиват хемолитична анемия, която носи името на пароксизмална нощна хемоглобинурия. В основата на това състояние е соматична мутация PIG-А, разположен на X хромозомата на хемопоетични стволови клетки.
Видео: Регулатори на вода и сол обмен
продукт е необходимо този ген за синтез на гликозилфосфатидилинозитол която осигурява фиксиране на клетъчната мембрана около 20 протеини, включително FSD и CD59. Един пациент с генетичен дефицит на изолиран CD59 беше слаб хемолитична анемия, въпреки нормален израз на FSD на мембраната. Напротив, когато изолиран генетичен дефицит FSD хемолитична анемия не се развива.
Пациенти с SLE и техните семейства са намерени частично (най-вероятно наследствена) невъзможност допълнение рецептор 1 (РК1). Това може да повиши риска от серумна болест (имунен комплекс болест), и по този начин да играе роля в патогенезата на SLE.
В серозни течности Настоящото протеаза, който унищожава С5а и IL-8, които служат като хемоатрактанти за неутрофили. В фамилна средиземноморска треска липсва тази протеаза намерени в перитонеалната и синовиалната течност. Пациентите са имали миссенс мутация на гена, кодиращ фактор на транскрипция на Пирин. Те страдали чести пристъпи на треска, придружени от болезнено възпаление на ставите, плеврит и перитонит. Очевидно, С5а, IL-8 или както обикновено се образуват върху повърхността на серозен и серозен течност съдържа инхибитор на тези хемоатрактанти, което предотвратява развитието на възпалителния отговор.
 Afibrinotenemiya angiohemophilia и новородените. Хеморагичен заболяване на новороденото
Afibrinotenemiya angiohemophilia и новородените. Хеморагичен заболяване на новороденото Влияние на декомпресия на фактори на кръвосъсирването. Фактор Хагеман декомпресия
Влияние на декомпресия на фактори на кръвосъсирването. Фактор Хагеман декомпресия Коагулация с кесонна болест. декомпресия феномен
Коагулация с кесонна болест. декомпресия феномен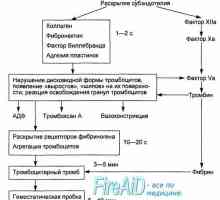 Вътрешна Path инициира съсирване. Ролята на калциеви йони в коагулацията
Вътрешна Path инициира съсирване. Ролята на калциеви йони в коагулацията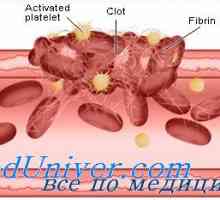 Лизис на кръвни съсиреци, плазмин. повишено кървене
Лизис на кръвни съсиреци, плазмин. повишено кървене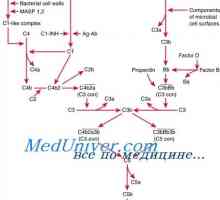 Алтернативен път на активиране на комплемента. Мембрана атака комплекс на комплемента
Алтернативен път на активиране на комплемента. Мембрана атака комплекс на комплемента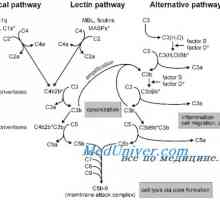 Класическият път на активиране на комплемента
Класическият път на активиране на комплемента Моноцистоза и лимфоцитоза. системата на комплемента
Моноцистоза и лимфоцитоза. системата на комплемента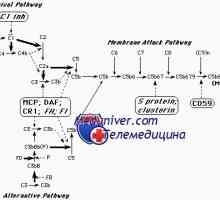 Нарушенията на системата на комплемента в гломерулонефрит, анемия, инфекции
Нарушенията на системата на комплемента в гломерулонефрит, анемия, инфекции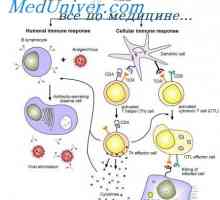 Оценка на фагоцитарната функция. Откриване на нарушения в системата на комплемента
Оценка на фагоцитарната функция. Откриване на нарушения в системата на комплемента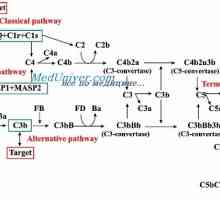 Оценка на системата на комплемента. Основният недостатък на компонент на комплемента
Оценка на системата на комплемента. Основният недостатък на компонент на комплемента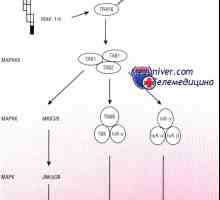 Схема IRF път в отговор на бактериите на чревния епител
Схема IRF път в отговор на бактериите на чревния епител Схема МАРК пътя в отговор на бактериите на чревния епител
Схема МАРК пътя в отговор на бактериите на чревния епител Имунодефицити в недостатъчност JAK3, ил-7ra, rag1 или rag2, CD45
Имунодефицити в недостатъчност JAK3, ил-7ra, rag1 или rag2, CD45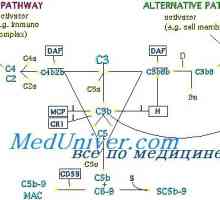 Регулаторните механизми на комплемента. Защитни функции на комплемента
Регулаторните механизми на комплемента. Защитни функции на комплемента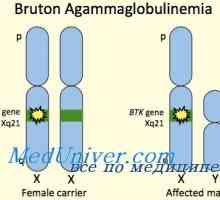 Х-свързана агамаглобулинемия. Brutonovskaya агамаглобулинемия деца
Х-свързана агамаглобулинемия. Brutonovskaya агамаглобулинемия деца Клетъчен имунен отговор. Хуморалния имунен отговор. Защитни функции на имуноглобулини (антитела).
Клетъчен имунен отговор. Хуморалния имунен отговор. Защитни функции на имуноглобулини (антитела). Хипертония причина далак протеини?
Хипертония причина далак протеини? Определяне на протеин С система активност с
Определяне на протеин С система активност с Тромботични заболявания: причини, лечение
Тромботични заболявания: причини, лечение Мембранозен гломерулонефрит: прогноза, лечение, симптоми, причини, симптоми
Мембранозен гломерулонефрит: прогноза, лечение, симптоми, причини, симптоми