Кортизол и надбъбречните андрогени

Съдържание
Видео: хормона на стреса - кортизол. Как да получавате част от ендорфини?
Биосинтезата на кортизола и надбъбречните андрогени
стероидогенезата
Основните хормоните на надбъбречната кора са кортизол, алдостерон и андрогени.
Синтез път на надбъбречните стероиди са пояснени чрез анализиране стероидогенезата ензими. Повечето от тези ензими, принадлежат към семейството на Р450 оксидази. P450 ензимаВКС (CYP11A кодиран от гена, разположен върху хромозома 15) разцепва страничната верига на холестерола. R450s11 ензим (кодиран от гена CYP11 един, разположен на хромозома 8) катализира хидроксилирането 1 11 11-дезоксикортизол и деоксикортикостерон (DOC), съответно, за да се образува кортизол и кортикостерон в областите на окото и гредата. Клетките на CYP11 ген зона гломерулоза 2 (също локализиран на хромозома 8) кодира ензим R450aldo (алдостерон синтаза), който катализира 11-хидроксилиране, 18-хидроксилиране и окислението-18 11-OK, превръщайки го в кортикостерон и по-нататък - до 18-хидроксил sikortikosteron и алдостерон. Всички тези реакции се провеждат в митохондриите на клетките. В ендоплазмения ретикулум P450c17 ензим (кодиран от ген CYP17, разположен на хромозома 10) има 17 -gidroksilaznoy и 17,20-лиаза дейности. Тук R450s21 ензим (CYP21A2 ген, кодиран) хидроксилиране прогестерон и 17-хидроксипрогестерон 21-ия въглероден атом. W и -gidroksisteroiddegidrogenaznoy 5.4-изомераза има същата микрозомалните ензими, които не принадлежат към семейството на цитохром P450.
Zone и стероидогенезата
Поради разликите в ензимите гломерулни и две вътрешни зони на надбъбречните функции кора като две жлези, които са различно регулиран и секретират различни хормони. Така че, в гломерулна зона, производство на алдостерон, не е 17-хидроксилаза и следователно не може да бъде синтеза на 17 ° С-17 -gidroksiprogesterona hydroxypregnenolone и е прекурсор на кортизол и надбъбречните андрогени. Синтезът на алдостерон клетки на тази зона се регулира ренин-ангиотензиновата система и калий.
Beam и нетните зони произвеждат кортизол, андрогени и малко количество естроген. Тези зони се регулира главно АСТН. Те не са изразени CYP11V2 ген (кодиращ R450aldo) и следователно превръщането на 11-OK в алдостерон невъзможно.
Абсорбция и синтез на холестерол
Синтез на кортизол и андрогени в гредата и нетни зони (както и синтеза на други стероидни хормони) започва с холестерол. Основният източник на холестерол за надбъбречните жлези са плазмените липопротеини, въпреки че холестерола се синтезира от ацетат и в самите надбъбречните жлези. Холестеролът дял идва от LDL, което представлява 80% от резервите си в надбъбречните жлези. При стимулиране на тези жлези бързо стероиди са синтезирани от малко количество на свободен холестерол. Едновременно с активиран хидролиза на складирани холестеролови естери, улавяне липопротеин амплифицира от плазмата и ускорява синтеза на холестерол от ацетат. Това бързо отговор, медииран регулиране на стероидогенезата малък протеин (звезда) - митохондриална фосфопротеин, който ускорява холестерол транспорт от външната към вътрешната митохондриална мембрана. Звезда генни мутации в основата вродена надбъбречна хиперплазия Lipoid, вече при раждането се характеризира с тежък дефицит на кортизол и алдостерон.
метаболизма на холестерола
Реакция, ограничаване на скоростта на стероидогенезата в надбъбречните жлези, е превръщането на холестерол прегненолон, и че тази реакция е основната цел на АСТН влияние. Той се среща в митохондриите и включва две хидроксилиране, последвано от отцепване на страничната верига на холестерола. Всички тези трансформации са катализирани от един ензим - CYP11A. Всеки етап изисква присъствието на кислород и електронна двойка, която служи като донор на NADPH. Флавопротеин adrenodoxin прехвърля тези електрони до протеин adrenodoxin желязо и сяра му CYP11A. Както adrenodoxin и adrenodoxin участва в реакция, катализирана от CYP11B1. Прехвърлянето на електрони за цитохром Р450 микрозомален случва с Р450 редуктаза (различни флавопротеин). Прегненолон образуван от допълнителни трансформации трябва да напусне митохондриите.
Синтезът на кортизол
синтеза на кортизол се предхожда от 17-хидроксилиране на прегненолон да образуват -gidroksipregnenolona 17 под действието на ензима CYP17 в гладка ендоплазмения ретикулум. След това 5,6-двойната връзка в 17 -gidroksipregnenolone превръща в 4,5-двойна връзка под действието на ензима комплекс W-хидроксистероид дехидрогеназа: 5.4-oksosteroidizomerazy, което също е локализиран в гладкото ендоплазмения ретикулум. Алтернатива (по-малко значими) реакция, протичаща в областта на лъча, намалява превръщането на прегненолон на прогестерон и допълнително - 17 -gidroksiprogesteron.
На следващия етап, който отново се появява в микрозоми и катализирана CYP21A2, е 21-хидроксилиране на 17 -gidroksiprogesterona да образуват 11-дезоксикортизол. Това съединение се подлага на 11-хидроксилиране в митохондрии (CYP11B1) за образуване на кортизол. Гредата и областите на окото са оформени като 11-добре, 18-gidroksidezoksikortikosteron и кортикостерон. Въпреки това, както е отбелязано по-горе, липса в тези зони CYP11B2 митохондриален ензим премахва възможността за синтеза на алдостерон в тях. В базови условия (т.е. в отсъствието на стрес) диапазони проценти секреция на кортизол 8-25 мг (22-69 тМ), средно 9.2 мг (25 микромола) на ден.
Видео: кортизол и спорта
синтез на андрогени
Образование надбъбречните андрогени от прегненолонът и прогестерон изисква предварителна хидроксилиране 17 (CYP17), което е невъзможно в гломерулната района. Най-големият размер на андроген се образува чрез превръщане на съединение -gidroksipregnenolona 17 до 19 въглеродни атома - DHEA и DHEA-сулфат. Микрозомният 17,20-дезмолаза (CYP17) отделя от 17 -gidroksipregnenolona страничната верига две въглен при 17-позиция, което води до образуването на DHEA, който съдържа кетогрупа в С17. DHEA при sulfokinazy превръща в DHEA-сулфат (обратима реакция). Друг надбъбречната андроген, андростендион, образувани главно от DHEA (под действието CYP17) и евентуално на 17 -gidroksiprogesterona (също под действието CYP17). Андростендион може да се превърне тестостерон, въпреки че надбъбречните жлези отделят минимални количества от него. Сами по себе си, надбъбречните андрогени (DHEA, DHEA-сулфат, андростендион) имат много слаба активност андроген и мъжествени на тези съединения се дължи на тяхната периферна превръщане в по-активен андроген - дихидротестостерон и тестостерон. DHEA и DHEA-сулфат се секретират от надбъбречните жлези в големи количества от андростендион, но качествено последният е по-важно, тъй като е по-лесно се превръща в периферията на тестостерон. Напоследък беше показано, че синтезата на някои стероидни хормони среща в нервната тъкан и сърцето, когато те са, както изглежда, като паракринен или автокринни фактори. Стероидогенезата ензими (например, W-хидроксистероид дехидрогеназа и ароматазни) са изразени в много тъкани.
регулиране на секрецията
Секрецията на CRH и АСТН
АСТН, тропен хормон за светлина и окото надбъбречните зони е основен регулатор на кортизол и надбъбречната андроген производство. Въпреки това, регулирането на тези процеси играе роля, и вещества, произведени в самите надбъбречните жлези - невротрансмитери, невропептиди и азотен оксид. Секрецията на АСТН, от своя страна, се регулира на ЦНС и хипоталамуса, където произведени невротрансмитери, кортикотропин освобождаващ хормон (CRH) и аргинин вазопресин (AVP). Невроендокринна контрол на секрецията на CRH и АСТН постига чрез три механизма.
Ефектът на АСТН на надбъбречната кора
Още по време на първите минути след прилагането на АСТН повишава нивото на стероид в плазмата. Надбъбречните жлези повишени синтеза на РНК, ДНК и белтък. Хронична стимулиране на АСТН води до хиперплазия и хипертрофия на надбъбречната кора, и обратно - дефицит АСТН инхибира стероидогенезата и се придружава от надбъбречната кора атрофия, намаляване на тежестта на тези жлези и протеини и нуклеинови киселини в него.
ACTH и стероидогенезата
CRF се свързва с висок афинитет към техните рецептори на плазмената мембрана на клетките на надбъбречната кора, което води до активиране на аденилат циклаза и увеличаване на количеството на сАМР в клетките. Последното от своя страна активира вътреклетъчни протеин кинази и звезда. Увеличаването на холестерол естераза активност, инхибира синтеза на холестерол естери и увеличава улавяне липопротеин надбъбречната кора. Всичко това ускорява образуването на свободен холестерол и взаимодействието му с ензим разцепва на страничната верига (P450scc или CYP11A1) за образуване A5-прегненолон. Тази реакция, както вече бе отбелязано, ограниченията на скоростта на стероидогенеза.
} {Модул direkt4
невро-ендокринна регулация
кортизол секреция строго контролирана АСТН и концентрация на кортизол в плазмата ниво АСТН варира паралелно. Невроендокринна кора регулиране надбъбречната състои от три механизма: 1) епизодични секреция и регулиране на дневните ritma- 2) взаимодействие на хипоталамо-хипофизо-надбъбречната (НРА системата) за стрес-3) инхибиране на АСТН кортизол секреция от механизъм за обратна връзка.
- Денонощен ритъм. От епизодични секрецията на кортизол денонощен ритъм, наложено определено на централната нервна система, която регулира количеството на емисиите и амплитуда секреторна CRH и АСТН. Секрецията на кортизол, ниско в късните вечерни часове, продължава да намалява през първите часове на съня. Тогава тя започва да се повишава, но след като се събуди отново пада. За максимална секреция на кортизол до около половината от общата дневна количество. На фона на постепенно намаляване на кортизол в следобедното галопиращи по-ниска амплитуда, свързани с приема на храна и физическата активност. Динамика на кортизол секреция може да се различават значително от човек на човек и дори в същото лице в зависимост от естеството на съня, цикъл светло-тъмно и времето на хранене. Циркадния ритъм секреция също се променя във физическия (тежка болест, операция, нараняване или глад) и психологически стрес (страх, ендогенна депресия, маниакална фаза на маниакално-депресивна психоза). Това е нарушена и патологични процеси в централната нервна система и хипофизната жлеза, синдром на Кушинг, кортизол метаболитни промени, хронична бъбречна недостатъчност, и алкохолизъм. Ципрохептадин като antiserotoninergicheskim ефект потиска циркадианния ритъм на кортизол секреция, но други лекарствени вещества обикновено не го променят.
- Реакция на стрес. АСТН и плазмените нива на кортизол са повишени в първите минути на операция или понижаването на нивото на глюкоза в плазма удължено стрес елиминира денонощен ритъм на секреция на тези хормони. Отговор на стреса започва в централната нервна система и е придружена от повишена секреция на CRH и АСТН. Преди приложение на глюкокортикоиди, както и техните подобрени ендогенни продукти в синдром на Къшинг, блокира АКТХ и кортизол отговор на стреса. Напротив, след адреналектомията ACTH отговор на стреса се засилва. Регламентът на системата HPA е ангажиран и имунната система. Например, интерлевкин-1 (IL-1) стимулира секрецията на АСТН и кортизол блокира IL-1 синтез.
- Инхибиране с механизъм за обратна връзка. Третият механизъм за регулиране на секрецията на АСТН и кортизол е да инхибира секрецията на глюкокортикоиди, които от отрицателно действие механизъм за обратна връзка на хипоталамуса и хипофизата. Това им действие се осъществява по два начина.
Бързо спиране на АСТН секреция зависи от скоростта на повишаване на нивото на глюкокортикоидите, но не и тяхната доза. Реакцията протича бързо (по време на първите минути), кратка продължителност (по-малко от 10 минути), и се медиира, изглежда мембрана отколкото класическите цитозолни глюкокортикоидни рецептори. Забавени и по-продължително потискане на АСТН секреция зависи от времето на действие на глюкокортикоидите, и техните дози. При продължителен прием на ниво глюкокортикоиди ACTH продължава да пада и губи чувствителност към стимулиране влияния. В крайна сметка това води до пълно спиране на отделянето на CRH и АСТН и атрофия на греди и ретикуларни зони на надбъбречната кора. Това потискане на системата НРА се осъществява, както изглежда, чрез класическите глюкокортикоидни рецептори.
Ефект на АСТН за производството на андрогени
Производство на надбъбречните андрогени при възрастни също се регулира от АСТН. Ежедневно ръб секреция на DHEA и андростендион съвпада с тези на АСТН и кортизол. АСТН бързо повишава нивата на DHEA и андростендион в плазмата и глюкокортикоиди намаляване на съдържанието им. DHEA-сулфат се метаболизира бавно и следователно е през деня плазменото ниво е стабилен. За дълго време, ние приехме, наличието на специално хормони от хипофизната жлеза, която регулира секрецията на надбъбречните андрогени, но това не е потвърдено.
Метаболизмът на кортизола и надбъбречните андрогени
В хода на техния метаболизъм тези стероиди загубят активност и, образувайки конюгати с глюкуронова киселина и сярна разтворимост придобива вода. Неактивни спрегнати съединения лесно се екскретират в урината. Steroid метаболизъм и конюгиране среща предимно в продукцията урина pecheni- 90% от тези метаболити.
Метаболизма и отделянето на кортизол
Преди неговото елиминиране на кортизол в урината претърпява различни трансформации. В непроменено производството на по-малко от 1% от секретиран кортизол.
Преобразуване в черния дроб
Сред метаболитни трансформации на кортизол в черния дроб най-важно, от количествена гледна точка, е необратимо инактивиране от 4-редуктаза, която регенерира 4,5-двойната връзка на пръстен А. Продуктът от тази реакция digidrokortizol, под действието на 3-gidroksistero iddegidrogenazy превръща в тетрахидрокортизол. Значителни количества кортизол и се подлага на действието на 11 - gidroksisteroiddegidro дехидрогеназа, става биологично неактивен кортизон, които под въздействието на ензими, споменати по-горе се образува tetragidrokortizon. Тетрахидрокортизол и tetragidrokortizon може да стане kortoevye киселина. Всички тези трансформации предизвика отделяне на приблизително равни количества кортизол и кортизон метаболити. В метаболизма на кортизол и кортизон също така са оформени и kortoly kortolony и (в по-малка степен) друго съединение (например, 6 -gidrokortizol).
Конюгирането в черния дроб
Над 95% от кортизол и кортизон метаболит в черния дроб за образуване на конюгати с остатъци на глюкуронова киселина и сярна киселина и в тази форма се въвежда отново в кръвта, и се екскретира в урината. Количествено по-важно е конюгиране с глюкуронова киселина (в групата на хидро-ksilnuyu в Z-позиция).
Промени в клирънс и обмяната на веществата
На кортизол метаболизъм, много условия засягат. В детството и старостта, той се забави. Хронично чернодробно заболяване, придружено от намаляване на екскреция на метаболити на кортизол в урината, въпреки че плазмената концентрация остава нормално. В хипотиреоидизъм кортизол метаболизъм забавя и намалява неговата екскреция в урината. За хипертиреоидизъм, характеризиращ се с противоположни промени. Клирънсът намалява кортизол по време на пости и анорексия, както и по време на бременност (поради по-високи нива от DRG). При кърмачета 6 -gidrokortizol става все по-кортизол. Същото се случва по време на бременност, естрогени, чернодробни заболявания и други тежки хронични заболявания, както и под влиянието на лекарства, които индуцират синтезата на чернодробни микрозомни ензими (барбитурати, фенитоин, митотан, аминоглутетимид и рифампицин). Физиологичното значение на тези промени е малък. Въпреки това, те са придружени от намаляване на пикочния 17-gidroksikortikosteroidov урината. Тези условия и по-силни лекарства да повлияят метаболизма на синтетични глюкокортикоиди и чрез ускоряване на метаболизма и разрешение от тях може да се отрази на тяхната концентрация в плазмата.
Кортизолът и кортизон шънт
натриев калиев обмен в дисталния нефрона регулира от алдостерон. Този ефект се медиира бъбречна минералокортикоидни рецептори. В ин витро условия афинитет глюкокортикоид и минералокортикоидни рецептори на кортизол същото. Въпреки това, ин виво, дори малки промени в нивото на алдостерон промяна натриев калиев обмен в бъбреците, докато свободен и биологично активен кортизол лишени от такъв ефект, въпреки факта, че неговата концентрация в кръвта е много по-високи концентрации на алдостерон. Това ясно парадокс се обяснява с действието на вътреклетъчния ензим - 11-хидроксистероид дехидрогеназа тип 2 (11-HSD2), който превръща кортизол до неактивен кортизон и по този начин предпазва минералокортикоидни рецептори от кортизол взаимодействия. Въпреки това, при много високи нива на кортизол в кръвта (например, синдром на Кушинг тежка) се преодолее този защитен механизъм. Активирането на минералокортикоиден рецептор кортизол повишава извънклетъчния обем, хипертония и хипокалиемия. Активно вещество сладник (glitsirizinovaya киселина) инхибира 11-HSD2 кортизол и осигурява свободен достъп до бъбречна минералокортикоидни рецептори, което води до хипокалиемия и кръвното налягане. Освен това, в някои тъкани настоящото изоензим 11-хидроксистероид дехидрогеназа (11 HSD 1) превръщане на неактивен кортизон до кортизол. Експресията на този ензим в кожата обяснява ефективността на кортизон мехлеми. По-важното е, че 11-HSD 1 се изразява в черния дроб. По този начин, ако бъбреците инактивиран кортизол, кортизон в струговане, че е възможно обратния процес в черния дроб. 11-HSD1 експресия в мастната тъкан може да обясни развитието на абдоминално затлъстяване и метаболитен синдром, в които нивата на кортизол не са повишени.
Метаболизма и екскрецията на надбъбречните андрогени
По време на метаболизъм настъпва надбъбречните андрогени или тяхното разпадане и инактивиране или превръщане в по-активните съединения - тестостерон и дихидротестостерон. В надбъбречните жлези се DHEA лесно се превръща DHEA-сулфат, който принадлежи на първо място сред андрогени, секретирани от тези жлези. Черният дроб и бъбреците и трансформира DHEA сулфат в DHEA или 4-андростендион. DHEA-сулфат или екскретира от бъбреците в непроменена форма или се превръща в 7-16 и хидроксилирани производни и след намаляване на 17-та позиция - в 5-и ростендиол сулфат. Андростендион или тестостерон се трансформира, или (след редукция на 4,5-двойната връзка) в etioholanolon или андростерон, от който чрез редукция на 17-та позиция са оформени съответно etioholandiol и ростендиол. целеви андроген тъкани, тестостерон се намалява до 5-позиция, се превръща в дихидротестостерон, които след vosstanavleniju ZA позиция форми ростендиол. Метаболитите на андрогени под формата на глюкурониди или сулфати се екскретират в урината.
 Вродена надбъбречна хиперплазия. Лечение на надбъбречна хиперплазия.
Вродена надбъбречна хиперплазия. Лечение на надбъбречна хиперплазия. Спешна помощ в надбъбречната недостатъчност: епидемиология на заболяването
Спешна помощ в надбъбречната недостатъчност: епидемиология на заболяването Синтез на адренокортикални стероиди. Минералкортикоид и глюкокортикоид
Синтез на адренокортикални стероиди. Минералкортикоид и глюкокортикоид Надбъбречните хормони. минералкортикоидната дефицит
Надбъбречните хормони. минералкортикоидната дефицит Синтезът на надбъбречните хормони. Стероидите са производни на холестерол
Синтезът на надбъбречните хормони. Стероидите са производни на холестерол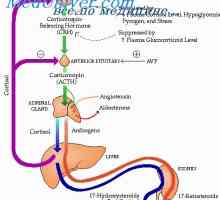 Регулирането на кортизол секреция. ACTH и неговата роля
Регулирането на кортизол секреция. ACTH и неговата роля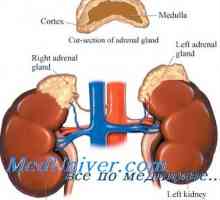 Физиология на надбъбречната кора. Надбъбречните хормони и тяхната функция
Физиология на надбъбречната кора. Надбъбречните хормони и тяхната функция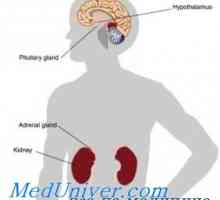 Вирилизиращи вродена надбъбречна хиперплазия: причини и механизми за развитие
Вирилизиращи вродена надбъбречна хиперплазия: причини и механизми за развитие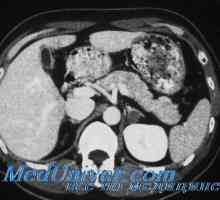 Средно алдостеронизъм. Gormonalnoaktivnye тумор на надбъбречната кора
Средно алдостеронизъм. Gormonalnoaktivnye тумор на надбъбречната кора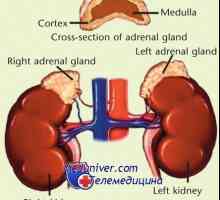 Надбъбречна недостатъчност: причини, клинична и диагностика
Надбъбречна недостатъчност: причини, клинична и диагностика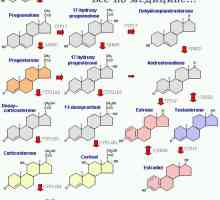 Стероидогенезата. Механизми за синтеза на стероиди
Стероидогенезата. Механизми за синтеза на стероиди Надбъбречните жлези
Надбъбречните жлези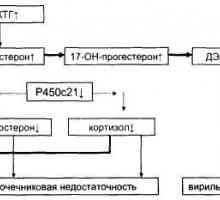 Особено вродена надбъбречна хиперплазия
Особено вродена надбъбречна хиперплазия Разграничаване доброкачествени и zlokachestvennyeref = "des204.htm"> надбъбречните…
Разграничаване доброкачествени и zlokachestvennyeref = "des204.htm"> надбъбречните… Хирзутизъм и вирилизация
Хирзутизъм и вирилизация Надбъбречните жлези в HIV
Надбъбречните жлези в HIV Надбъбречните жлези
Надбъбречните жлези Надбъбречните и яйчниците хиперандрогения: причините, лечение, симптоми, признаци
Надбъбречните и яйчниците хиперандрогения: причините, лечение, симптоми, признаци Надбъбречната вирилизация
Надбъбречната вирилизация Cindromy причинено от прекомерна секреция на докинг
Cindromy причинено от прекомерна секреция на докинг Стероидогенезата в яйчниците
Стероидогенезата в яйчниците