Фоликул физиология и менструален цикъл

Съдържание
На менструалния цикъл се управлява от сложно взаимодействие между хипоталамо-хипофизо-яйчниците ос и матката.
Ако опишете накратко този механизъм в хипоталамуса произвежда гонадотропин-рилизинг хормон (GnRH), който стимулира производството на LH и FSH от хипофизната жлеза. Гонадотропини инициира процеса на съзряване на овоцита в яйчника. Успоредно с това, яйчниците секретират хормона, които влияят върху ендометриума, тя се подготвя за имплантиране. В допълнение, на яйчниците хормони, въз основа на ефекта на обратна връзка на хипоталамуса и хипофизата, регулиращи секрецията на гонадотропини по време на менструалния цикъл. Всичко това сложно взаимодействие се обсъжда в подробности по-долу.
Хипоталамус-хипофиза система
GnRH е основен инициатор на репродуктивната функция. GnRH е пептид от 10 аминокиселини с кратък полуживот на 2-4 минути. Тя се формира в специални секретиращи неврони, които се появяват в процеса на развитие на обонятелната плоча и след това мигрират към mediabazalny хипоталамуса. Тези неврони, разположени в средната издигането и секретират специфичен режим GnRH импулс ( "импулсен генератор") в портала съдове, които GnRH достига gonadotrofy намира в аденохипофизата. GnRH се свързва с рецептори, принадлежащи към суперфамилията на G-протеин-свързан рецептор трансмембранен semidomennyh. 1,4,5-трифосфатаза и акт диацил-глицерол като вторични посредници за GnRH. Честотата на пулсация на секрецията на GnRH е регулиран синтез и секреция на гонадотропини от хипофизата.
По време на фоликуларната фаза на бавно освобождаване на GnRH - всеки 90-120 минути - активира секреция на FSH. В отговор на стимулиране с FSH, фоликул зреене в яйчниците отделя естрадиол. Този хормон извършва отрицателна обратна връзка и инхибира освобождаването на FSH, GnRH продукти медиирана намаляване чрез неврони, които съдържат гама-аминомаслена киселина, в допълнение към това, може да има пряк ефект върху хипофизата. Естрадиол участва в положителна обратна връзка, която увеличава честотата на пулсация на GnRH за 60 минути в фоликуларната фаза, а също така директно стимулира секрецията на LH от хипофизната жлеза. LH стимулира яйчниците, така че да има по-нататъшно увеличение на естрадиол секреция. Въпреки, че в този момент не е бърза промяна на пулсациите на GnRH, естрадиол и други регулаторни механизми за увеличаване на хипофизата чувствителност към GnRH. Това увеличение на чувствителността води до бързо увеличаване на производството на LH (пик LH), който стимулира овулацията. След овулацията разкъсания фоликул (жълтото тяло) произвежда прогестерон. Този хормон е включен в отрицателната обратна връзка, повишаване на ендогенната опиоидна активност и може директно да се намали честотата на пулсация GnRH 1 импулс в продължение на 3-5 часа. По този начин се увеличава FSH синтез през прехода лутеалната-фоликулите. Както скоростта на намаляване повишава концентрацията на прогестерон GnRH пулсация, която спомага за освобождаването на FSH.
Ролята на хипофизната жлеза
Gonadotrofy подредени в аденохипофиза и представляват priblizitelno10% от общия фонд на клетките на хипофизата. Тези клетки синтезират и секретират LH и FSH. Тези хормони и тироид-стимулиращ (TSH) и човешки хорионгонадотропин (ЧХГ) принадлежат към семейството на глико-протеин хормони. Гонадотропини - функционални хетеродимери и се състои от алфа и бета субединици. Аминокиселинната последователност на алфа субединицата е идентично за всички гликопротеинови хормони, като бета субединица се характеризира с различен състав на аминокиселина, и съдържа уникална информация.
Синтез на FSH и LH най-често се среща в същите клетки. секреция на FSH е тясно свързано с експресията на бета субединицата. Има предположение, че в gonadotrofah е минималният състав на FSH, и голямата част от него се отделя от конституционното начин. LH секреция случва по различен начин: първо LH се натрупва в органели, и след това под действието на фактор на спусъка се извършва освобождаване (пътека корекция). Различните олигозахариди на бета субединица могат да предоставят вътреклетъчен сортиране, в резултат на различни механизми на секреция.
Диференциално експресиране на гените, което води до производството и освобождаването на гонадотропини аденохипофизата клетки зависи от GnRH и яйчниците хормони чрез механизми за обратна връзка. Бавно честота GnRH пулсация увеличава експресията на Р-субединицата на FSH производството и увеличава амплитудата А G. Обратно, увеличаването на пулсации честота GnRH активира експресията на бета субединица на LH, повишаване на освобождаването на FSH. В резултат на това, амплитудата на LH се намалява, а средната концентрация в плазмата се увеличава. По този начин, ефектът на полови стероиди на пулсациите на GnRH косвено контролира производството на предния дял на хипофизата гонадотропини.
В vnutrigipofizarnoy мрежа няколко механизми играят важна роля в синтеза и секрецията на гонадотропини. Gonadotrofy синтезират и секретират пептиди, принадлежащи към семейството на трансформиращи растежни фактори (TRF). Активин е местен регулаторен протеин, който участва в контрола на gonadotrofov на функция. Бавно пулсация на GnRH стимулира синтеза на активин, което от своя страна увеличава транскрипцията на FSH. Бързо пулсация на GnRH стимулира производството на фолистатин, друг TRF-свързан протеин, който се свързва активин. Това намалява бионаличността на FSH синтез и активин намалява съответно. В допълнение към местните регулаторни механизми за експресията на гонадотропини повлияе на яйчниците растежни фактори като трансформиращ инхибин.
Ролята на яйчниците
Яйчниците са тясно свързани с процеса на регулиране на менструалния цикъл чрез механизми за обратна връзка. В допълнение, на яйчниците съдържат вътрешната мрежа, включително фактори, които са синтезирани локално и действат като паракринен и автокринни регулатори гонадотропен активност. Чрез intraovarialnym регулатори включват семейството на инсулин-подобен растежен фактор (IGF) семейство и суперсемейство TRF епидермален растежен фактор (ЕБФ). Освен това, тези фактори са включени в координиране на развитието на фоликулите, овулацията и стероидогенеза.
яйчниците менструален цикъл включва фоликуларен и лутеалната фаза. Фоликуларната фаза се характеризира с растежа на доминантен фоликул и овулацията. Тя обикновено е 10-14 дни. Въпреки това, тази фаза може да варира значително с течение на времето и зависи от дължината на менструалния цикъл при овулация жена. Лутеалната фаза започва веднага след овулация и е период, когато яйчниците произвеждат хормони, които могат да подкрепят евентуална имплантация. Продължителността на тази фаза е относително постоянна средно на 14 дни (12-15 дни). Фаза на менструалния цикъл, ще бъдат описани по-подробно в следващия раздел.
Първични фоликули са основната репродуктивна единица, включваща басейн на "спане" на овоцити. Морфологично те се състоят от първични ооцити заобиколени от един слой на гранулозно сквамозноклетъчен и базално мембрана. Те нямат кръвоснабдяване. Тези първични фоликули се развиват между 6 и 7 месец на бременността и представлява пълен състав на яйчниковите фоликули.
Folikulyarnoe развитие започва с преход "сън" изконни космените във фазата на растеж. Точните механизми, които контролират първоначалното въвеждане на фазата на растеж изначалната фоликул все още не е изследвана до края. Предполага се, че басейнът на останалите фоликули под постоянен тоник "инхибиране" контрол. Основно процес на зреене води до индуциране на растежа на някои първични фоликули, а съседните фоликули остават неактивни в продължение на месеци и дори години. Предполага се, че постепенното активиране на фоликули е дълъг процес, който започва веднага след формирането на ембрионални клетка басейн и завършва с изчерпването на фоликуларен единица. Този сложен процес не зависи от гонадотропини. Въз основа на няколко проучвания предполагат, че включването на процеса на изначалната развитието на фоликулите отговаря система интраовариалните предупреждение, която включва някои от членовете на семейството на РФ. Известно е също, че за правилния растеж и развитие на изначално
фоликул клетка изисква близък контакт с гранулознотекални клетки и яйцеклетката. Тези клетки чрез междина мостове connexin семейство пас и от ооцитите от различни фактори, хранителни вещества и продукти на разпадане.
Има теория, че самата яйцеклетка се отразява смъртта му, секретиращи различни фактори. Този процес включва производството на два растежни фактори, свързани с TRF- са произведени от ооцити в ранното развитие на фоликулите, растеж диференциращ фактор (RDF) -9 и костен морфогенен протеин (BMP) -15. В проучване на с рецептори увреждания мишки са показали, че ооцитите активира гранулозни клетъчна пролиферация чрез тези растежни фактори в отговор на гранулозните клетки произвеждат фактори (например, фолистатин, кит лиганд), които намаляват инхибиторен ефект (например, Inhibin А, Мюлерови инхибиране вещество) и допринасят за стимулиране на растежа на яйцеклетка.
Към днешна дата, се описват редица местни фактори, така и в бъдеще ще се намери по-голям брой от тях. Продължава проучването на тези растежни фактори и хормони ще помогне да се определи физиологията на процеса на съживяване на първични фоликули. Брой на терминалните клетки е ограничено, и всяка пълна узряване на фоликулите намалява резервни клетки. Всяко заболяване, което води до намалена терминал клетка или ускори активирането на фоликул може да доведе до ранната фоликулярна изчерпване и по този начин до преждевременно прекратяване на репродуктивната функция.
Развитие на първичен фоликул е първият етап от растежа на фоликулите. Основно фоликул, от изначалните няколко различни функции. Събиране на яйцеклетки започва да расте. Част от процеса на растеж е образуването на бистър зона (зона пелуцида). Състои се от дебел слой на гликопротеини, които са най-вероятно синтезирани яйцеклетка. Този слой напълно обгражда ооцита и бариера между клетките ооцита и гранулозните. Тя изпълнява редица функции, необходими за защита и торене на яйцеклетката. В резултат на гранулозните клетки се подлагат на серия от морфологични промени на плоския на кубичен. Тази стъпка развитие може да продължи до 150 дни.
Преходът към вторични фоликули се случва, когато размера на яйцеклетката максимална (120 нанометра в диаметър), гранулозни клетъчна пролиферация и появата на капсулните клетки. Точният механизъм на наличието капсулните клетки недостатъчно проучени, но се предполага, че те са формирани от съседни яйчниците мезенхим (стромални фибробласти), както тя се движи в мозъка на развиващия се фоликул вещество яйчниците. Развитието на този слой дава възможност за образуване на вътрешна и външна Текето. С развитието на фоликул тека клетка получава захранване с кръв, въпреки факта, че слоят гранулознотекални клетки не остане vaskulyarizirovanymi. Гранулозните клетки произвеждат вторичен фоликул на FSH рецептори, естроген и андроген. Този етап може да отнеме до 120 дни, може би това е поради дългия период удвояване гранулозните клетки (>250 часа).
По-нататъшно развитие води до образуването на третичен фоликул антрални или ранна фаза. Този етап се характеризира с образуването на кухина, или кухини в фоликула. Антрални течност съдържа стероиди, протеини, електролити, протеогликани, както и ултрафилтрат, който се формира чрез дифузия през основната плоча. Този етап се характеризира също чрез по-нататъшно диференциране на капсулните клетки. Субпопулациите капсулните-интерстициални клетки се развиват в рамките на вътрешния тека съдържат рецептори за LH и осигуряват клетка стероидогенеза. След това започва диференциацията на гранулозните клетки. Тъй като основната плоча, клетките се разделят на групи, както следва: мембрана periantralny слой яйценосен нарастък и корона радиата. Развитието влияния производство на FSH и неидентифицирани сигнали, получени от яйцеклетката. Предполага се, че факторът на яйцеклетка-зависим (RDF-9) е неразделна част от процеса. Промяна на концентрацията на RDF-9 влияе на образуването на слой. Също така, гранулозни клетки в отговор на стимулиране с FSH произвеждат активин, която е член на мазнини. Активин се състои от две субединици варианти: А и В, които са свързани помежду си чрез дисулфидни връзки. Различни комбинации от тези субединици поражда различни активин (активин А [А, А] AB [A, B], или IV [V, В]). Напротив, активини не хормони, тъй като тяхната концентрация в кръвта е постоянна и е независима от менструалния цикъл и неговата свободна фракция в кръвта не е определен. Основната роля на aktivinina е активиращ рецептор на FSH в гранулозните клетки и повишаване на фоликулогенезата.
Растежът в началото на антралните фоликули фаза се извършва при бавно и постоянно темпо. Фоликулите достигнат диаметър от 400 пМ. първичен фактор на растеж на фоликулите на този етап е FSH-стимулирани гранулозните клетки на митози. До този момент оцеляването и растежа на фоликулите са до голяма степен независими от гонадотропини. В предпубертетна възраст и при жени, приемащи противозачатъчни средства, за този етап фоликули са в различни етапи на развитие. На този етап от фоликул за тяхното по-нататъшно развитие и растеж, трябва да имате FSH. Ако няма достатъчно на FSH, фоликули претърпяват обратно развитие.
Морфологично единица - фоликул, състояща се от капсулните и гранулозните клетки е независима единица на хормон, който е отговорен за производството на естроген. Тека и гранулозните клетки са под прякото въздействие на LH и FSH, съответно. Гонадотропини увеличаване на производството и активността на транскрипционен фактор FS-1 сАМР в съответните клетки. В тека клетки, изложени на LH се увеличава LH-рецептор на клетъчната повърхност и повишена експресия и активност звезда, P450scc, RR-HSD-II, P450c17 необходим за подобряване на андрогенно производство. FSH увеличава производството на гранулозните клетки ароматаза и 17р-HSD.
Андрогените могат да бъдат получени по един от двата начина: D5 път, при което като се използват DHEA прекурсорния и пътя D4 - андрогенния синтез на 17-ОН-прогестерон. Въпреки това, човешки D4 пътека е представено с минимум. Това се дължи на факта, че 17,20-лиаза има много по-голям афинитет към 17-ОН-прегненолонът от 17-ОН-прогестерон. Така, основната прекурсор на полови хормони при хора е DHEA.
Андрогените, главно андростендион, преминават през фоликула основната плоча и се превръща в основен прекурсор на естрогени. Естрадиол биосинтетичен път, определен от тип 17р-HSD. Мъжът е идентифициран седем вида на 17р-HSD, всяка от които има афинитет към някои стероиди. В гранулозните клетки, основно представени 17р-HSD тип 1, което намалява естрон молекула, превръщане в естрадиол. 17р-HSD тип 3 се открива главно в Лайдиговите клетки и подпомага преминаването на андростендион в тестостерон. 17р-HSD тип 5 е в капсулните клетки и също така насърчава прехода на андростендион в тестостерон. Така основният начин на естрадиол биосинтеза се провежда в гранулозните клетки по време на ароматизиране на андростендион до естрон, включващи ароматаза и последваща редукция на естрон с естрадиол молекули, включващи 17р-GSD1 тип 1.
Видео: Най-менструалния цикъл е 2/2
} {Модул direkt4
Необходимостта да участват в естрадиола фоликулите, както и механизмите на положителна и отрицателна обратна връзка на хипофизната жлеза достатъчно проучени. Въпреки това, ролята на естроген в местния процес на съзряване и израстване на фоликула остава спорен. Очевидно е, че естроген са синергични с FSH в фоликуларната фаза, защото те увеличават рецепторна експресия на LH и FSH стимулира пролиферацията на гранулозните клетки, и да усили активността на ароматазата. Въз основа на проучване, проведено върху мишки с увреждания на ароматазата, че се предполага, ролята на местната естроген. Главно тези мишки имали големи антрални фоликули, но след една година той не е разкрил някакви антрални фоликули или вторични и изначалната подложиха атрезия. Въпреки това, тези мишки овоцити могат да узреят ин витро и да образуват бластоцист. Очевидно е, че има естрогенни рецептори в гранулозните клетки и капсулните клетки. Изследвания при мишки с увреждания -estrogenovymi рецептори са показали, че тези мишки са безплодни и нямат graafovyh мехурчета. В този случай, мишката с увреждания -estrogenovymi рецептори са в състояние да се раждат деца. При хората, има случаи на развитие на фоликулите в отсъствие на естрадиол секреция в тялото. Такъв случай се наблюдава при жени с дефицит от CYP 17а, който фоликул растеж беше белязан с въвеждането на гонадотропини. В ин витро оплождане е маркиран растеж на ембриона, но, за съжаление, не е имало случай на бременността.
Vnutriovarialnye фактори играят решаваща роля и в двата фоликула и в стероидогенезата. Овоцита произвежданите фактор RDF-9 освободен през фоликулогенезата на процеса. Смята се, че този фактор не само работи гранулозни клетки диференциация, но също така има стимулиращ ефект върху капсулните клетки и инхибиране на образуването на жълтото тяло клетки. Изследвания ин витро показват, че IRF-1 и IRF-2 повишава пролиферацията на гранулозните клетки и естрадиол секрецията. Въпреки това, че се предполага, че в процеса на съзряване на фоликул доминиращата роля на изпълнявана от IGF-2, а не IGF-1. Този факт може да се обясни с липсата на експресия на IGF-1 в гранулозните клетки на доминантен фоликул. Освен това, жени със синдром Laron (липса на IGF-1) е възможно овулацията стимулация с гонадотропини. Този факт показва, че наличието на IGF-1 не е необходим фактор в фоликул.
гранулозните клетки произвеждат други хормони, които регулират фоликулогенезата, например, синтезирано субединица които субединица се свързва и образува хетеродимери известни като Inhibin А (А) или Inhibin B (B). Ролята на инхибин в стероидогенезата на фоликул и непряко, чрез потискане на производството на FSH от хипофизната жлеза. Концентрацията на инхибин А и В са зависими от менструалния ритъм. Оборотният инхибин А ниво се повишава в края на фоликуларната фаза и остава високо във всички Teneev lyutey-нова, а концентрацията на инхибин Б огледално отражение на концентрацията на FSH. Въпреки че нивата на инхибин на серумните увеличава съответно увеличаване на размера на гранулозните клетки в отговор на стимулиране с FSH в фоликуларен инхибин концентрация не зависи от размера на фоликула. Предполага се, че концентрацията на серумния инхибин Б отразява сумата на гранулознотекални клетки и може да служи като показател за растежа на яйчниковия резерв. Тъй инхибин В е основен инхибитор на продукцията на FSH от хипофизната жлеза на фоликуларната фаза в отсъствие на естрадиол, измерване на основните нива на FSH може да бъде непряко маркер на яйчниковия резерв.
Антрални фаза се характеризира с интензивен растеж на фоликулите (1-2 mm / дневно) и зависи от концентрацията на гонадотропини. В отговор на FSH стимулиране на антрални фоликули се увеличава бързо и достига до 20 mm в диаметър, главно поради натрупване на течност антрални. Тека клетки продължават да се диференцират в интерстициална, които произвеждат по-голям брой на андростендион за последващо ароматизиране на естрадиол. гранулознотекални клетки продължават да се разграничат една от друга. Мембранен слой под влиянието на FSH придобие рецептори за LH. Това се различава от мембрана слой кумулативен слой, в който не LH рецептори. Крайният развитието на зрял фоликул е селективен процес, при който най-често се оказва един доминантен фоликул готов за овулация.
Процесът на подбор започва в средата на лутеалната фаза на предишния цикъл. Повишена естроген предизвиква усилване предварително овулационен FSH-активност във фоликула, а на принципа на обратната връзка затруднява производството на хипофизната FSH. Намалена хипофизната секреция на FSH води до преустановяване на гонадотропин за подпомагане малки антрални фоликули, което води до тяхното атрезия. Въпреки спада на концентрацията на FSH, доминантния фоликул продължава да расте, увеличаване на масата на гранулозните клетки с голям брой рецептори за FSH. Повишени васкуларизация капсулните клетки осигурява селективно доставяне на FSH на доминантен фоликул, въпреки намаляването на серумните концентрации на FSH. Повишените нива на естроген в космения улеснява активиране на рецептор LH гранулозни клетки фоликулостимулиращ хормон, който позволява на фоликула да отговори на овулация освобождаване на L G. При липсата на естрогенни рецептори на LH гранулозните клетки не се развиват върху повърхността.
LH вълна е абсолютно условие за овулация и узряването на ооцитите. Засилено производство на LH в средата на цикъла се дължи на повишена чувствителност на хипофизата да GnRH. Чувствителност се дължи на положителната обратна връзка между експоненциални концентрации на растеж и естроген може инхибин А. В резултат на това освобождаване става възстановяването на мейозата на яйцеклетката I за освобождаване на полярен тялото непосредствено преди овулацията. Има основание да се предположи, че гранулозните клетки секретират узряването на ооцитите инхибитор (ISO), който взаимодейства с Кумулус на кумулус и по този начин блокира мейотичен процеса по време на фоликулогенезата. Теоретично, се счита, че ISO оказва своето въздействие, като блокира освобождаването на цАМФ в Кумулус оофорус, която прониква в незрялата яйцеклетка мейотичен съзряването и спира. LH вълна надхвърля ISO блокиране действие, намаляване на концентрацията на сАМР и увеличаване на вътреклетъчната концентрация на калций, което позволява да се възобнови мейоза.
Непосредствено преди овулация, увеличаване на производството на прогестерон, който може, в частност, и е причина за върха на FSH в средата на цикъла. Peak FSH стимулира производството на адекватни количества LH рецептори на гранулозните клетки. FSH, LH и прогестерон индуцира експресията на протеолитични ензими, които разграждат колагена в фоликуларен стена и вредни. Увеличава производство прогестерон, така че може би има намаляване на гладкомускулни клетки, които увеличават изгонването на яйцеклетката.
Пик на ЛХ трае около 48-50 часа. 36 часа след началото на освобождаването на LH се случва овулацията. Сигналът за обратна връзка за спиране излъчването на А Т неизвестен. Може нарастващи концентрации на прогестерон негативен механизъм за обратна връзка инхибира секрецията на хипофизата GnRH чрез намаляване на пулсации честота. Непосредствено преди овулация също потиска LH активност собствени рецептори, които намаляват хормон активност на функционални единици. В резултат на намаленото производство на естрадиол.
След овулация, и в отговор на LH, гранулозни клетки и интерстициалните капсулните клетките, останали в зрели фоликула диференцират в granulezo- и капсулните лутеин клетки, съответно, с образуване на жълтото тяло. LH и предизвиква производството на съдовия ендотелен растежен фактор (VEGF), който играе важна роля в развитието на жълтото тяло на съдовата мрежа. На новообразуваните съдове проникват в базалната мембрана, и през активиран прогестерон биосинтеза на LDL в гранулозните-лутеин клетки. След овулация активира LH рецептори в лутеалната клетки, използвайки неизвестен механизъм. Това е ключов фактор в поддържането на базалната LH за запазване на жълтото тяло.
За лутеум хормон необходимо взаимодействие тека лутеин и гранулозните-лутеин клетки, както и в предварително овулационен фоликула. В отговор на LH и ЧХГ, на капсулните лутеин клетки за подобряване на експресията на ензими, участващи в синтеза на андростендион. В гранулознотекални лутеин клетки, с участието на LH повишава активността на ароматазата за ароматизиране на андрогени в естрогени. Основната разлика между гранулозните-лутеин клетките на преовулаторната гранулозните клетки е да индуцира експресия на P450scc и Sp-HSD, които позволяват на клетките да синтезират прогестерон. секреция
Прогестерон и естрадиол се появява спорадично и е свързано с нарастване на LH. FSH има минимално въздействие върху производството на прогестерон, обаче, той продължава да се стимулира производството на естрадиол в лутеалната фаза. прогестерон концентрация се увеличава и достига своя връх на около 8-ия ден на лутеалната фаза, която продължава около 14 дни.
Процесът на обратно развитие на жълтото тяло (програмирана клетъчна смърт) започва около 9 дни след овулацията. Механизми на инволюция на жълтото тяло не е напълно изяснен. Веднага след като lyuteolizis започва бърз спад в концентрациите на прогестерон. Въз основа на няколко проучвания, може да поеме ролята на естроген в lyuteolizise. Това е показано чрез директно администриране на естроген в яйчниците, съдържащ жълтото тяло. Това може да се направи въз основа на експериментални данни, предположението, че точно преди lyuteolizisom в жълтото тяло е процес на активиране на ароматаза дейност. Увеличете ароматаза дейност възниква в отговор на стимулация с гонадотропини (LH и FSH), докато в лутеалната фаза, най-вероятно, FSH играе голяма роля. По този начин, има спад в активността на Sp-HSD. Тази редукция може да доведе до намаляване на концентрацията на прогестерон и съответно да lyuteolizisu. Освен това, местните модулатори, като окситоцин, произведени от жълтото тяло клетки участват в синтеза на прогестерон. Други изследователи подкрепят ролята на простагландини в Люта-лиза. Експериментални данни показват, че PGF2a, който се секретира в матката или яйчниците по време на лутеалната фаза, стимулиращи цитокини, такива като тумор некрозис фактор (TNF), в резултат на апоптоза, която се проявява и като следствие, разграждане на жълтото тяло.
Известно е, че протеолитични ензими, участващи в lyuteolizisa процес. Предполага се, че в процеса на lyuteolizisa повишена активност на матрични металопротеинази. Генериране на известен модулатор на матрични металопротеинази е ЧХГ. Този факт може да играе важна роля в ранните етапи на бременността, когато ЧХГ пречи на жълтото тяло регресия. Въпреки това, в отсъствието на жълтото тяло на бременност се намалява, което води до намаляване на концентрацията на прогестерон, естрадиол и инхибин А. Намаляването на концентрацията на тези хормони води до увеличаване на пулсация GnRH и FSH секреция. Увеличаването на концентрацията на FSH стимулира Следващото поколение на фоликули и предизвиква нов менструален цикъл.
Ролята на матката
Основната функция на матката е поставянето и поддържането на плода живот. Ендометриума - вътрешния слой на матката, който се различава по време на менструалния цикъл, така че да може да запази и подхранване на ембриона. Хистологично ендометриума представени епител образуване жлеза и изграждане мина, която съдържа стромални фибробласти и извънклетъчна матрица. Ендометриума морфологично разделя на два слоя: базалната и функционални. Базалния слой пряко граничи миометриума и включва простатата, както и в подкрепа на съдовете. Тя доставя компоненти, необходими за развитието на функционалната слой. Функционалният слой е динамичен слой, който регенерира всеки следващ цикъл. В този слой може да се появят бластоцисти на имплантация.
По време на менструалния цикъл, ендометриален развитие настъпва в отговор на стимулиране на яйчниците с хормони. Подобно на други ендокринните органи, матката съдържа множество локални фактори, които модулират хормонална активност. Фаза ендометриума координира с овулация фази. По време на фоликуларната фаза, фаза на пролиферативен ендометриума преминава. Тя започва в началото на менструацията и завършва с овулацията. По време на лутеалната фаза ендометриума преминава секреция. Тя започва през овулацията и завършва точно преди менструация. Ако имплантация не се случва, идва дегенеративно фаза. В тази фаза преминава менструация. Следваща фаза на ендометриума ще се счита за по-подробно.
По време на фоликуларната фаза, естрогени са Яйчниците произвеждат които стимулират жлези в базалния слой за формиране на функционален слой. Естрогените са допринесли за увеличаване на експресията на гени на различни цитокини и растежни фактори, включително ORF, TRFos и IGF. Растежни фактори създават микросреда, в рамките на ендометриума да усили ефекта на хормоните. В началото на менструалния цикъл, ендометриума е тънка, обикновено по-малко от 2 мм. Ендометриума жлези и тънки линии, и изпратени от базалния слой на вътрешната повърхност на маточната кухина. Както стромата и ендотела появи естроген и прогестерон рецептори. Вити кръвоносните съдове от базалния слой чрез прилив на съединителна тъкан, за да се поддържа притока на кръв към ендометриума. В крайна сметка функционален слой покрива цялата маточната кухина и достига 3-5 mm дебелина (обща дебелина 6-10 mm). Този етап се нарича пролиферативно.
След овулация, яйчника произвежда прогестерон, което инхибира допълнително пролиферация на ендометриума. Тези механизми могат да бъдат приложени, използвайки антагонисти на естрогенните рецептори. Прогестеронът деактивира естрогенни рецептори и подпомага метаболизма на естрадиол в ендометриума чрез стимулиране активност 17р-HSD превръщане на естрадиол и по-малко активен метаболит на естрон. По време на лутеалната фаза на жлезист епител гликоген натрупва и започва да секретират гликопептиди и протеини в маточната кухина. Това е течен субстрат, който поддържа свободното движение на която е в бластоциста. Прогестеронът също стимулира диференциацията на ендометриума и предизвиква хистологичните промени. Жлези стават значително по-усукване, спирални съдове стават още по-усукани и да приемат формата на тирбушон. Stroma става много оточни води до повишаване на капилярната пропускливост. Клетките изглеждат уголемени и многостенни. Този процес се нарича predetsidualizatsiya. Тези клетки са много активни и реагират добре на хормонални импулси. Те произвеждат простагландини, заедно с други фактори, които участват в менструация, имплантацията и бременността. Тази фаза се нарича отделителната.
Ако няма имплантацията на ембриона, тя започва дегенеративно фаза. Естрогените и прогестерон предизвикват производството на простагландин PGF2a и PGE2. Простагландините от своя страна причиняват прогресивно вазоконстрикция и релаксация на спирала съд. Вазомоторни реакции причиняват ендометриума исхемия и реперфузионно увреждане. Накрая, в ендометриума развива кървене с образуване на хематом. Прогестеронът активира ММР активност води, които допринасят за деградацията на извънклетъчната матрица. Както прогресията на исхемия-TION и разграждане, некротизиращ функционален слой и се изхвърля заедно с менструацията като кръв и ендометриума. Кръв загуба по време на нормална менструация е около 25 до 60 мл. Въпреки факта, че PGF2a е мощен стимулатор на миометриума и по този начин намалява следродилна кървене, той не влияе на менструално кървене. Основният механизъм участва в ограничаването загуба на кръв се тромбин тръба и естроген-свързан рана отново епителизация през базалния слой на ендометриума, което започва в ранната фоликулярна фаза на следващия менструален цикъл.
Ако има концепция, имплантация може да се случи в ендометриума в средата на секреторната (лутеална) фаза. По това време на ендометриума има достатъчна дебелина и доставката на хранителни вещества. Синцитиотрофобласт директно секретират ЧХГ, който съхранява и поддържа секреция на прогестерон на жълтото тяло, необходима за пълното развитие на ендометриума децидуа.
По този начин, две фази преминава яйчниците по време на менструалния цикъл: фоликуларен и лутеална. Ендометриума - трите фази, които са синхронизирани с фазите на яйчниците. Тези сложни механизми за обратна връзка между яйчниците и оста хипоталамус-хипофиза регулират менструалния цикъл. По време на фоликуларната фаза, яйчниците секретират естрадиол, който стимулира ендометриума. След овулация (лутеалната фаза) яйчниците произвеждат естроген и прогестерон, които активират изправяне на ендометриума и се подготвят за секреторна фаза. В един цикъл не сложи край на бременността се развива lyuteolizis, което води до прекратяване на производството на хормони. Тази версия почивка хормон води до дегенеративни фаза и началото на менструацията.
Видео: Най-менструалния цикъл. Хормони. овулация
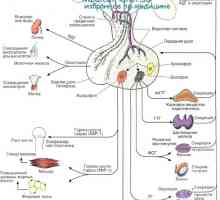 Физиологията на хипофизната жлеза. хипофизни хормони
Физиологията на хипофизната жлеза. хипофизни хормони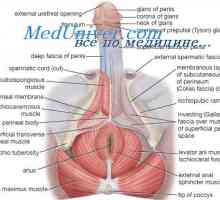 Регламентът на сексуалните функции на мъжкото тяло. Гонадотропин-освобождаващ хормон
Регламентът на сексуалните функции на мъжкото тяло. Гонадотропин-освобождаващ хормон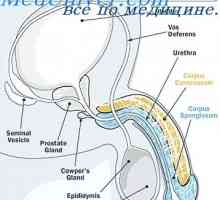 Потискането на синтезата на мъжки хормони. регулиране на сперматогенезата
Потискането на синтезата на мъжки хормони. регулиране на сперматогенезата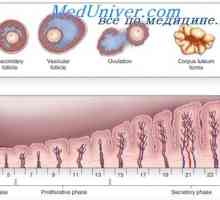 Месечен цикъл на яйчниците. Функции на гонадотропини
Месечен цикъл на яйчниците. Функции на гонадотропини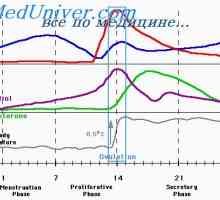 Регламент на женската сексуална месечен курс. Женските полови хормони
Регламент на женската сексуална месечен курс. Женските полови хормони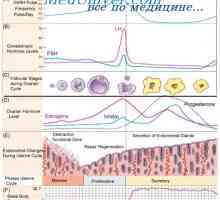 Овулация хормони. Хипоталамо-хипофизната-яйчниците
Овулация хормони. Хипоталамо-хипофизната-яйчниците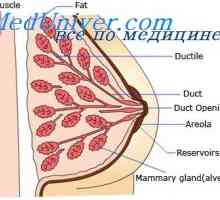 Регламент на пролактиновата секреция. Разделяне на млякото под действието на окситоцин
Регламент на пролактиновата секреция. Разделяне на млякото под действието на окситоцин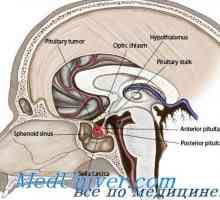 Фоликулостимулиращ хормон FSH
Фоликулостимулиращ хормон FSH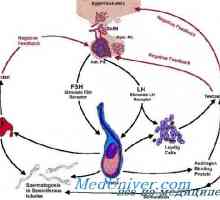 Хипоталамуса. Освобождаващ гонадотропин хормон функция (GnRH)
Хипоталамуса. Освобождаващ гонадотропин хормон функция (GnRH)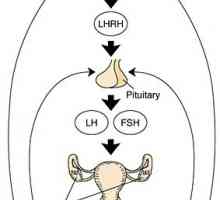 Хипоталамус-хипофиза-яйчниците система. характеристики възрастови
Хипоталамус-хипофиза-яйчниците система. характеристики възрастови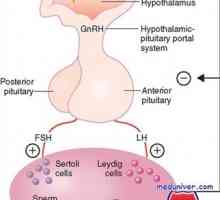 Гонадотропин-освобождаващ хормон (GnRH). Функции и Синтез
Гонадотропин-освобождаващ хормон (GnRH). Функции и Синтез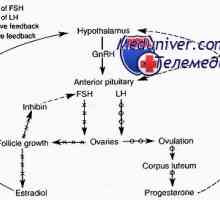 На яйчниците като ендокринен орган. теория две клетки
На яйчниците като ендокринен орган. теория две клетки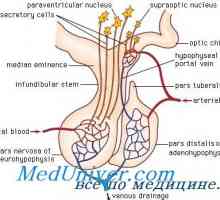 Inhibin и актинвин функция. фолистатин
Inhibin и актинвин функция. фолистатин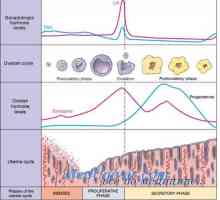 Лутеалната фаза на менструалния цикъл. регулиране
Лутеалната фаза на менструалния цикъл. регулиране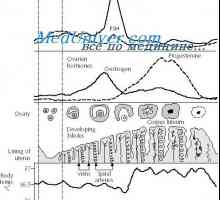 Преходът на лутеалната-фоликуларната фаза на менструалния цикъл. регулиране
Преходът на лутеалната-фоликуларната фаза на менструалния цикъл. регулиране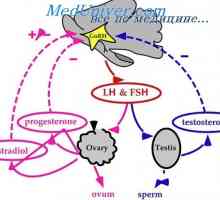 Механизми за началото на пубертета. Значение на мастната тъкан
Механизми за началото на пубертета. Значение на мастната тъкан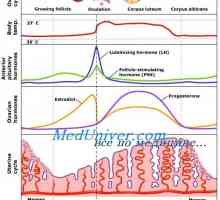 Овулаторния фаза на менструалния цикъл. регулиране
Овулаторния фаза на менструалния цикъл. регулиране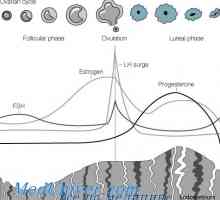 Регулирането на менструалния цикъл. Хормони фоликуларната фаза
Регулирането на менструалния цикъл. Хормони фоликуларната фаза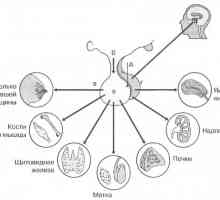 Хипофизата и хипоталамуса
Хипофизата и хипоталамуса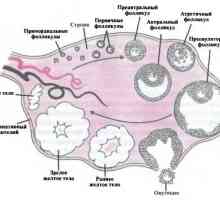 Анатомия и физиология на женската полова референтна система
Анатомия и физиология на женската полова референтна система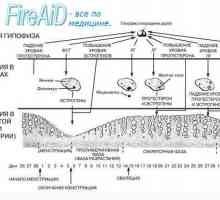 На менструалния цикъл (цикъл на матерен разтвор). Фаза на менструалния цикъл. Менструалния фаза.…
На менструалния цикъл (цикъл на матерен разтвор). Фаза на менструалния цикъл. Менструалния фаза.…