Група 1 (подгрупа 1а) - алкален метал (основна лента)
Той включва Li, Na, К, Rb, Cs, Fr (Таблица. 1 и 2). За много химични свойства малко по-различни от другите алкалните метали Ли+, като диагонал прилика Mg2+.
Таблица 1. Някои химични и физични свойства на алкални метали
име | Am. номер | Това се отнася, при. тегло | E формула | Радиус ч | Основни изотопи (%) | |
Ли | Литиево Lithium [от гръцки. Lithos - камък] | 3 | 6.941 | [Той] 2sл | Ли+ 78, 152 атомни ковалентно 123 | 6Li (7,5) 7Li * (92,5) |
Na | Натриев Натриев [Eng. Soda- броня. Натрий] | 11 | 22.9898 | [Ne] 3sл | Na+ 98 атомна 153.7, ван дер Ваалс 231 | 23Na * (100) |
K | Калиев Калиев [Eng. Potash- броня. Калий] | 19 | 39.0983 | [Аг] 4sл | K+ 133, 227 атомни ковалентно 203 | 39К * (93,26) 40K (0012) 41 К * (6.73) |
Rb | Рубидиев Рубидиев [от шир. rubidius - тъмночервен] | 37 | 85.4678 | [Кр] 5sл | Rb+ 1.49 атомен 247.5, ван дер Ваалс 244 | 85Rb * (72,17) 87Rb * (27,83) |
Cs | Цезиев цезиев [от шир. Caesius - светлосиня] | 55 | 132.905 | [Хд] 6sл | Cs+ 165, атомен 265.4 ковалентно 235 | 133Cs * (100) |
Fr | Франций Франций [след Франция] | 87 | 223 | [Rn] 7sл | Fr+ 180 | 223Fr * (следи) |
Литий (Li) е сред най-ниските на всички плътност метали - 0,53 гр / см3, с ниска активност реагира с кислород и вода. Това е стратегически метал отбранителната промишленост. Той се използва под формата на сплави с Al и Mg в производството на водородни бомби, като част от смазочни масла, емайли, батерии, stekla- използва в медицината.
Литиево от алкални метали най-токсични. подготовка Ли2CO3 се използва в медицината за лечение на маниакално-депресивна психоза. При продължително излагане на лекарството дава бъбреците и централната нервна система. Ето защо, с повишено съдържание Ли в кръвта и урината се смята за признак на бъбречна дисфункция. Освен това, значително количество резултати катион в заместването на магнезий с литий в Mg2+-зависими ензими, например, ензими на гликолиза.
Натриев (Na) - лек метал, сребро бяло на разреза бързо окислява. Той реагира бурно с вода. Големите количества, използвани в промишлеността, по-специално в топлообменниците на ядрената reaktorov- съставени NaCl широко използвани в хранителната и химическата промишленост.
Отнася се за жизнено важни елементи. Възрастен човек съдържа около 100 г натриев, 30% от тях - в костите. В съединенията има валентност на едно и КН координационни съединения (който образува редки натрий) е обикновено равна 6. неорганични натриеви соли са разтворими във вода, за да образуват съответните йони. Някои натриеви соли с органични киселини, например, соли на пикочната киселина и винена киселина (тартарати и урат) слабо разтворимо.
Na+ е основният междуклетъчен катион регулиране електролитна хомеостаза, активността на транспорт натриев помпа през биомембрани аминокиселини, захари, различни аниони ПРИРОДА поддържане на осмотичното налягане и рН, кръвен CO2 (Под формата на бикарбонат) хидратирани разтворимост протеин (разтваряне) на органични киселини. Излишният натрий в диетата причини претоварване хомеостаза системи електролитни и дехидратиран тъкан. Клинично тя се проявява развитие, по-специално хипертония.
Калий (К) - мека бял метал реагира с кислород и вода. Тя се използва в производството на торове в химическата промишленост, за топене на стъкло.
Отнася се за жизнено важни елементи. Възрастен човек съдържа около 140 гр калиев, 98% - в клетките. Неговите координационни съединения в валентността, равни на 1, и зависи от броя координация на лиганда. K+ Това е най-важното междуклетъчен катион. Необходимо е да се поддържа невромускулната възбудимост, вътреклетъчен осмотичното налягане и рН, мускулни контракции и осигуряване на пропускливостта на клетъчните мембрани. извънклетъчен K+ Той стимулира натриев помпата. натриево-калиев помпа в някои физиологични процеси йони K+ може да бъде заменен Rb+ и Cs+. Значителни количества последния елемент могат да се появят в тялото след излагане на радиация. Чрез реактивност е подобен на калиев Na+.
Na и K -2 основния метал осигуряване на електролитна хомеостаза. И двата елемента в живите организми определят осмотичното налягане от двете страни на клетъчната мембрана и са положителни противойони за отрицателни аниони (Cl-, НАП42-, НСО3- и органична).
Обикновено човек йони съотношение Na+/K+ кръв се колебае около стойност 1.5. Намалена концентрация K+ в цяла кръв и увеличаване в плазмата, свързани с нарушена пропускливостта на външната мембрана на клетката, обикновено непропусклив K+, или в нарушение на дейности Na+/K+ - за обмен на стъпка помпата вътрешната митохондриална мембрана. В нервните клетки, като прекъсване на тази помпа придружава от смущения на потенциала на мембрана неврони и нервните импулси върху него. Промени в съдържанието на йони на алкални метали, наблюдавани при много неврологични zabolevaniyah- описва развитието на хиперкалиемия когато парестезия, парализа и т.н.
Хипернатремия придружено от повишаване на кръвното налягане и едновременно приемане на високи калиеви храни (домати, портокали, спанак, банани) значително намалява вероятността от удар. Според Харвардското училище за обществено здраве, проведено наблюдение на 44 милиона американци, е намаляването достига 38%. Въпреки това, само полезен в умерен dozah- си излишък в кръвта най-често се наблюдава при заболявания на бъбреците. Продължителен съотношение прекъсване Na+/K+ Това води до сърдечно-съдови заболявания.
Рубидиев (Kb) - микроелемент примес. Човешкото тяло съдържа около 0.3 мг рубидий, обикновено в рамките на клетките (подобни на K+). Могат да образуват координационно съединение. Тъй като кинетиката и усвояването и механизма на участие в обмена са подобни на K, изотоп 86Rb използван при проучвания за споделяне K+. при дефицит K+ приемане рубидий възстановява киселина-алкален баланс. Rb бързо се елиминира от тялото през бъбреците.
Цезиев (CS) - биологични свойства, подобни на K+. При хора тя може да съдържа до 1,5 мг на цезий. В медицината се използва като етикет радиоактивен изотоп 137Cs (Време за полуразпад т1/2 = 30 години), както и стабилен изотоп 133Cs чрез ядрено-магнитен резонанс. Смята се, нетоксични.
Франций (Fr) - намерени в естествено състояние в много малки количества в уранови руди. Образувана от радиоактивното разпадане на актиния (с хелий). Поради малкия полуживот на всички изотопи на един елемент от недобре проучена. Трябва да бъде токсичен поради радиоактивност, въпреки че не е намерен в човешкото тяло.
Таблица 2. Съдържанието в тялото, токсични (TD) и летална доза (LD), алкален метал
Както кората (%) | В океана, (%) | В човешкото тяло | TD, LD | ||||
Средно (телесно тегло 70 кг) | Bone (%) | Мускулна (%) | Кръв (мг / л) | ||||
Ли | 2 * 10-3 | 17 * 10-6 | 0,67 мг | ND | 23 * 10-7 | 0004 | TD 92-200 мг, LD - ND |
Na | 2.3 | 1.05 | 100 гр | 1.0 | 0,26-0,78 | 1970 | нетоксичен |
K | 2.1 Видео: Химия - просто. урок 1 "PSE" | 379 * 10-4 | 140 гр | 0.21 | 1.6 | 1620 | TD 6 г, 14 г LD |
Rb | 9 * 10-3 | 12 * 10-6 | 680 мг | (0.1-5) * 10-4 | (2-7) * 10-3 | 1.49 | TD е малък, LD-ND |
Cs | 3 * 10-4% | 3 * 10-8% | ND | (13-52) * 10-7 | (7-160) * 10-6 | 0.0038 | нетоксичен |
Fr | 0% | 0% | ND | ND | ND | ND | ND |
Медицински bioneorganika. GK овца
 Водороден пероксид в панкреатит
Водороден пероксид в панкреатит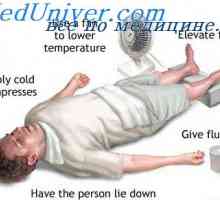 Топлинен удар спортисти. Компенсация за загуба на натриев и калиев хлорид при спортисти
Топлинен удар спортисти. Компенсация за загуба на натриев и калиев хлорид при спортисти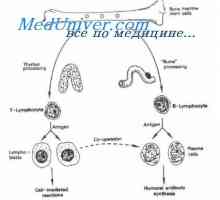 ИРНК участва в синтеза на антитяло. Методи за изучаване на иРНК
ИРНК участва в синтеза на антитяло. Методи за изучаване на иРНК Проби с натоварване на калиев Boyanovich. Определяне на натрий и калий в слюнката за оценка на…
Проби с натоварване на калиев Boyanovich. Определяне на натрий и калий в слюнката за оценка на…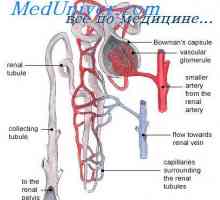 Механизмът на сол на апетита. Регулиране на тялото калий
Механизмът на сол на апетита. Регулиране на тялото калий Тиазидни диуретици. инхибитори на карбоанхидразата
Тиазидни диуретици. инхибитори на карбоанхидразата Метални импланти
Метални импланти Видове химични връзки
Видове химични връзки Обща информация за радиоактивното разпадане и йонизиращите лъчения
Обща информация за радиоактивното разпадане и йонизиращите лъчения За да фасцията на главата включва: времеви броня, престилка темпорален, дъвчене броня, престилка…
За да фасцията на главата включва: времеви броня, престилка темпорален, дъвчене броня, престилка… Вулвита възпаление на външни органи генитални прилагане често са свързани с вагинит (вж.…
Вулвита възпаление на външни органи генитални прилагане често са свързани с вагинит (вж.… Изгаряния гърлата обикновено се наблюдават в резултат на злополука, като у дома си. При възрастни,…
Изгаряния гърлата обикновено се наблюдават в резултат на злополука, като у дома си. При възрастни,… Лок Ringer (Solutio natrii chloridi composita-Solutio звънене Лок). Състав: 9 г натриев хлорид,…
Лок Ringer (Solutio natrii chloridi composita-Solutio звънене Лок). Състав: 9 г натриев хлорид,… Хоросан "Disol" "Trisol" "Acesol" "Chlosol"…
Хоросан "Disol" "Trisol" "Acesol" "Chlosol"… Калиев бромид (Kalii bromidum). Синоними: Калий bromatum, калиев бромид. Безцветни или бели лъскави…
Калиев бромид (Kalii bromidum). Синоними: Калий bromatum, калиев бромид. Безцветни или бели лъскави… Литиево елемент от групата на алкалните метали. Литиеви соли са били предложени за дълго време…
Литиево елемент от групата на алкалните метали. Литиеви соли са били предложени за дълго време… Калиев ацетат (Kalii asetas). Синоним: Калий aceticum. Бял кристален прах, без мирис или ниско…
Калиев ацетат (Kalii asetas). Синоним: Калий aceticum. Бял кристален прах, без мирис или ниско… Solimok (solimok). Вътрешен лекарство подобен по структура и действие на soluranu. Съдържа 46,3%…
Solimok (solimok). Вътрешен лекарство подобен по структура и действие на soluranu. Съдържа 46,3%… Една стъпка по-близо до органична електроника
Една стъпка по-близо до органична електроника Физикохимични свойства на лекарствен минерална вода
Физикохимични свойства на лекарствен минерална вода Класификация на интензивно миришещи вещества вещества. Теория за произхода на миризливите вещества
Класификация на интензивно миришещи вещества вещества. Теория за произхода на миризливите вещества