Onkologiya-
EI Podoltseva
Град болница номер 31, Санкт Петербург
източник RosOncoWeb.Ru
реакция "реакция на присадката срещу левкемия" след костен мозък allogennoyperesadkiИзползваните в последните години nonmyeloablative режими himioterapiipri трансплантация на хемопоетични стволови клетки на солидни тумори е lecheniyadisseminirovannyh логически zaversheniempochti петдесет години експериментални и клинични issledovaniyroli имунни механизми novoobrazovaniyallogennoy при лечението на злокачествен трансплантация на костен мозък.
Барнс и Loutit бяха първите, които описват ефекта на "transplantatprotiv левкемия" (TPL). През 1956 г. те показа, че мишки vyzhivaemostleykoznyh по-горе, и ако са извършени transplantatsiyaot алогенни здрави донори, в сравнение с трансплантация на мишки с левкемия poluchivshimisingennuyu.
Идеята за използване TPL ефект при хора за лечение на левкемия и izlecheniyaot алогенна трансплантация на костен мозък prinadlezhitGeorges Máthé, който за първи път през 1956 г., описва ефекта на TPL ubolnogo, получен за левкемия трансплантация kostnogomozga. През следващата трансплантация група от Сиатъл установено, че пациентите, които са били подложени на тежък свръхреакция "transplantatprotiv домакин" (GVHD), както и при пациенти с хронична RTPHimeli по-ниско ниво от рецидив в сравнение с пациенти, които не са имали тези усложнения. Въпреки това, ефектът на TPL soznachitelnoy асоциация и често фатални GVHD реакция entuziazmispolzovaniya ограничени GVHD провокации да се намали честотата retsidivovposle алогенна трансплантация на костен мозък.
В бъдеще, тази гледна точка е унищожена данни poluchennymiv две ключови изследвания. През първите големи серии транспланти, резултатите от които са анализирани международен регистър transplantatsiikostnogo мозък, беше установено, че пациенти с hronicheskimmieloleykozom (CML), които са получили костен мозък изчерпани Т-клетки (за предотвратяване на GVHD), вероятността от заболяване повторение uvelichivalasv 7 пъти в сравнение с тези, които не са имали прояви на GVHD, трансплантация на костен мозък nesmotryana суров Т клетки. Etidannye демонстрира възможно липсата на мощен съобщение медиирани от лимфоцити, TPL ефект с развитието на GVHD (Harowitzi др., 1990). Чрез наблюдение Kolb и сътр. (1990, 1995) установяват, че при пациенти с рецидивирал CML след трансплантация на костен мозък, е възможно да се получи стабилна ремисия на получения инфузия donorskihlimfotsitov.
Инфузията на донорни лимфоцити също Porteri съавтори се прилага успешно (1999) за предизвикване на ремисия при пациенти с остър ihronicheskim левкемия, лимфом и миелом рецидив трансплантация posleallogennoy костен мозък, и в много (esline във всички случаи), злокачествени системни заболявания krovipodvergalis ефекти на TPL реакции.
реакция "реакция на присадката срещу тумор"
Има ли реална възможност за предизвикване на ефект analogichnyyTPL срещу не-хематологични тумори? Понастоящем vremeniustanovleno че в някои случаи, туморни метастази infiltriruyutsyaT клетки и тяхната регресия, очевидно, причинени от тези лимфоцити (Vose, Мур, 1985). Следователно, можем да предположим, че allogennyeT лимфоцити също може да повлияе тумор. Podtverzhdeniemsuschestvovaniya реакция "реакция на присадката срещу тумор"(ТРО) е фактът, че твърди тумори, произтичащи в organahi тъкани, които са прицелни органи на GVHD имат същото tkanespetsificheskieantigeny, които са еднакво изложени на нападение tsitotoksicheskimilimfotsitami.
През последните години, ние, произведени някои експериментални доказателства за съществуването на ТПО ефект. Така Morecki и Славин (1997, 1998) успешно генерира ТРО реакция в мишки с простатата adenokartsinomoymolochnoy след алогенна трансплантация. В същото време на лицата, които са получили алогенни клетки от далак, не razvivalismetastazy в белите дробове, както и значително увеличаване на степента на оцеляване vsledstvieeffektivnoy премахването на минималния allogennymikletkami остатъчно заболяване на. Резултатите, получени Bartels сътр (1996), показват също превенция на метастази legkihu мишки трансплантирани с клетъчна линия миелома MC-38 posleinfuzii алогенни лимфоцити, стимулирани с туморни клетки.
Алоимунна и автоимунна реакция антитуморна
До сега, достатъчен аргумент в podderzhkupredpolozheniya че алогенна имунната система okazyvaetbolee мощен TPO ефект от имунната система на реципиента. Първо, донори имунни клетки не са толерантността на туморни клетки, и дори ако такъв толерантност се развива след трансплантацията, има възможност за повторно фрактура пресни инфузии donorskihlimfotsitov до пълното унищожаване на тумора. Също така е възможно predvaritelnayavaktsinatsiya донорски специфични туморни антигени, които yavlyaetsyabolee ефективен от ваксиниране на пациента. На второ място, antigennyyrepertuar способен да предизвика имунен отговор антитуморно, много повече в алогенна трансплантация на и се увеличава с uvelicheniemantigennoy несъвместимост. Трансплантиран донор T kletkirazlichayut не само тумор-специфични антигени, но също така и алелни варианти на тези антигени kompleksagistosovmestimosti незначителни антигени, тъкан специфично експресиран retsipientom.V случай на несъвместимост антигени основния комплекс gistosovmestimostiopuholevye реципиентни клетки експресират също различни HLAantigeny. Разликите в HLA-C и HLA-DR при пациенти с алогенна трансплантация на"разпознаваема" естествен убиец донор kletkami.V резултат алогенна имунен отговор е значително повишен, например, HLA свързани haploidentical трансплантация ochischennyhot Т лимфоцити стволови клетки, които могат да bytvazhnym компонент ТРО ефект (Ruggeri и сътр., 1999).
Алогенните хематопоетични стволови клетки тумори prisolidnyh
Алогенните хематопоетични стволови клетъчни злокачествени заболявания prinegematologicheskih vypolnyalasnemnogimi изследователи поради висока смъртност при пациенти prietom метод за лечение. По този начин, двете групи ispolzovaliallogennuyu трансплантация на трансплантация на костен мозък в гърдата zhelezy.Pri това Eibl и колеги (1996) бяха първите, които описват effektTPO при жени с метастатичен рак на гърдата след химиотерапия vysokodoznoyradio доза с алогенна костно mozgaot отнасящ донор HLA-идентични. Авторите наблюдават znachitelnoeumenshenie чернодробни метастази, които развиват на фона на GVHD. Byloustanovleno че лимфоцитите в периода след трансплантацията proyavlyalispetsificheskuyu цитотоксична активност срещу клетъчни линии от рак rakamolochnoy, което потвърждава наличието на тумор-spetsificheskogoallogennogo отговор в пациент. Ueno и сътр (1998) izrakovogo център M.D. Anderson (САЩ) се използва също vysokodoznuyuradio химиотерапия трансплантация на костен мозък с алогенна mozgav лечение на пациенти с метастазирал рак на гърдата. Unekotoryh пациенти са получили отговор, вероятно obuslovlennyyTPO ефект, но процентът на смъртност при тази група пациенти, svyazannayas трансплантация е била висока. Наскоро Bay сътр (2000), получени резултати показват регресия opuholevoymassy и стабилна ремисия при пациенти с метастатичен kartsinomoyyaichnika след алогенна трансплантация и развитието на GVHD. Всички etirezultaty конфликт с данни, получени priallogennoy трансплантация при деца с невробластом. Висока chastotaretsidivov след висока доза химиотерапия и автоложни стволови клетки transplantatsiigemopoeticheskih пациенти с невробластома IVstadii Установено е свързан с замърсяване autotransplantataopuholevymi клетки. В това отношение, някои issledovateliprimenili алогенна трансплантация на костен мозък от HLA-донор identichnogorodstvennogo като алтернатива лечение bolnyhs невробластома (Kremens и сътр., 1997 Matthay и сътр., 1994 Moritakei др., 1998). Въпреки това, когато се сравняват резултатите от лечението autologichnoyi данни алогенен трансплантат за наличие на ТРО ефект poluchenone е. Тези предварителни данни показват, че ТПО chtopriroda степента и влиянието на различни тумори chrezvychaynovariruyut.
Не-миелоаблативна трансплантация на хематопоетични стволови клетки (NTGSK) за лечение на метастазен рак
Като се започне от концепцията за възможно много висока effektivnostireaktsii ТРО, няколко групи свят трансплантация popytalisproverit хипотеза, че при алогенна трансплантация eliminatsiyaopuholevyh клетки почти напълно може да бъде осигурена effektomTPO вместо висока доза химиотерапия. Този подход изисква primeneniyanemieloablativnoy имуносупресия при подготовка bolnogodlya трансплантация, като по този начин да присаждане transplantata.S тази цел се използват различни видове konditsionirovaniyas включване на антитимоцитен глобулин и по-малко от pristandartnoy алогенни трансплантации дози tsitostaticheskihpreparatov :. бусулфан, циклофосфамид и т.н. В бъдеще, когато primenenieflyudarabina pretransplant подготовка на пациенти показва, че лекарството е още по-мощен и chrezvych ино horoshoperenosimym имуносупресор. В допълнение, флударабин obladaetvelikolepnym антитуморен ефект в някои variantahleykozov. Смята се, че това е едно от лекарствата в развитието, което prinadlezhitbuduschee nonmyeloablative трансплантация (Славин, 2001) .Posttransplantatsionnaya имуносупресия за профилактика на GVHD bylaminimalnoy които са допринесли за бързото му и пълно система vosstanovleniyuimmunnoy и развитието на ТПО ефект. Впоследствие avtoryvypolnyali инфузия на донорни лимфоцити за допълнително obespecheniyareaktsii ТРО имунната система, дължащи се на превръщане 100% донор retsipientav (Barret, Childs, 2001). В резултат eksperimentalnogolecheniya твърди тумори като стратегия nonmyeloablative transplantatsiiimela очевидно предимство пред стандартните алогенни transplantatsieys използват интензивно (миелоаблативна) видове химиотерапия и лъчетерапия, при пациенти с метастазирал рак на който ненаблюдавано увеличение антитуморен отговор, дори при naraschivaniidoz химиотерапия. NTGSK се използва също при пациенти с metastaticheskoypochechno карцином и меланом. Тези тумори са vybranyiz тяхната имуногенност. В този случай, пациентите не отговарят на immunomoduliruyuschuyuterapiyu IL-2 или интерферон, стандартна химиотерапия е takzheneeffektivna. Авторите са се опитали да се подобри реакцията ТРО ispolzuyav на алографт на хематопоетични стволови kletkis висока концентрация на Т-лимфоцити. Въпреки пациентите бедните obschiystatus преди трансплантация, те са сравнително horoshoya с минимални токсични преместен predtransplantatsionnuyuhimioterapiyu. По време на първите 30 дни след трансплантацията priznakovprogressirovaniya заболяване при тези пациенти са имали не bylo.V последващо значителен ефект се получава в 10 от 19 пациенти, на които 3 - пълна ремисия с изчезването на всички лезии metastaticheskihochagov, 7 - частичен отговор. Ефектът на ТРО razvivalsyacherez 3-6 месеца след трансплантацията, обикновено след immunosupressivnogolecheniya циклоспорин на премахване и преместване на пациента от смесват до polnomuT-клетъчна химеризъм. Проявите на остро GVHD в тези bolnyhassotsiirovalis реакцията ТРО, обаче, един пациент bylapoluchena пълна ремисия без остра GVHD, и имат няколко bolnyhotmechalas регресия на заболяването след няколко месеца poslerazresheniya остра GVHD (Barret, Childs, 2001).
NTGSK също се извършва в 15 пациенти с метастатичен refrakternoymelanomoy (Barret, Childs, 2001). В същото време 12 пациенти са починали otprogressirovaniya заболяване, двама - от трансплантация усложнения svyazannyhs. PosleNTGSK степента на прогресиране на болестта при пациенти с метастатичен меланом vyzyvaetsomneniya ефективността на този метод на лечение (Barret, Childs, 2001).
Резултатите от лечението на солидни тумори, използвайки NTGSKsvidetelstvuyut на изключителна променливост ТРО ефект. В nastoyascheevremya няма ясни прогностични показатели, отговарящи на такова проучване ефективност на lechenie.Poetomu NTGSK при различни metastaticheskihopuholyah (включително сарком на мека тъкан, аденокарцином, epitelialnyeraki) се простира.
Причината за използване transplantatsiigemopoetichekih nonmyeloablative стволови клетки за лечение на пациенти metastaticheskimrakom са: 1) ниска смъртност (2.5%) в posttransplantatsionnomperiode (Barret и др, 2001), - 2) възможно въздействие върху opuholevyekletki устойчиви на интензивна химиотерапия поради reaktsiiTPO- 3). този метод на лечение е основа за имунотерапия dalneyshegorazvitiya злокачествени заболявания. Така че, poluchennyepervye резултати от лечение на пациенти с малигнен NTGSK novoobrazovaniyamisvidetelstvuyut на негативното въздействие на имуносупресия на proyavleniyaeffekta ТПО. В тази връзка, наскоро предприетите rassmatrivayutsyasleduyuschie да развият това лечение:
1) пълно изключване posttransplantatsionnomperiode в имуносупресивната терапия поради отстраняването на алореактивни клетки трансплантация отговорни за GVHD;
2) успоредно с премахването на Т-клетки, отговорни за GVHD капацитет на концентрацията на присадка клетка, реагент stkanespetsificheskimi туморни антигени и определяне reaktsiyuTPO;
3) подобряване на идентификацията на туморни антигени, тумор-spetsificheskimitsitotoksicheskimi sootvetstvuyuschimantigenom лимфоцити от ваксинацията. И в далечното бъдеще - създаване spetsificheskihT туморни клетки, които дават възможност за адаптивна имунотерапия без подтискане на имунната система на хемопоетични стволови клетки (Barret, Чайлдс, 2001).
 Костно-мозъчна трансплантация спаси момчето от алергии
Костно-мозъчна трансплантация спаси момчето от алергии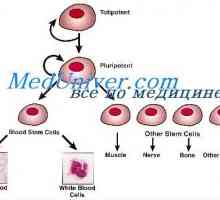 Самостоятелно подновяване на стволови клетки. В пролиферативна способност на стволови клетки
Самостоятелно подновяване на стволови клетки. В пролиферативна способност на стволови клетки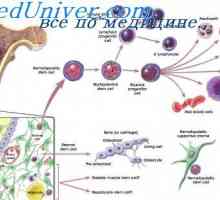 Лимфоидо прекурсори. Произходът на кръвни клетки
Лимфоидо прекурсори. Произходът на кръвни клетки Произход и микросредата клетки. Фибробласти на лимфоидни органи
Произход и микросредата клетки. Фибробласти на лимфоидни органи В-супресор клетки. Потискане на имунен отговор в лимфоцити
В-супресор клетки. Потискане на имунен отговор в лимфоцити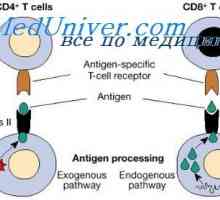 Характеристики сътрудничество имунни клетки. Хуморален фактор антитяло
Характеристики сътрудничество имунни клетки. Хуморален фактор антитяло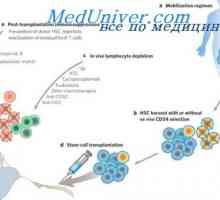 Разстройства на нервната система и растежа на злокачествени тумори след трансплантация на стволови…
Разстройства на нервната система и растежа на злокачествени тумори след трансплантация на стволови…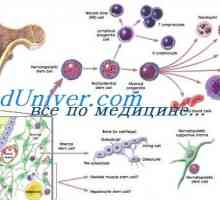 Кръв трансплантация на стволови клетки в апластична анемия
Кръв трансплантация на стволови клетки в апластична анемия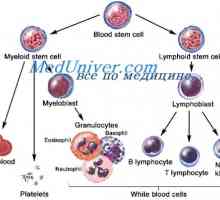 Трансплантация на стволови клетки на остра левкемия
Трансплантация на стволови клетки на остра левкемия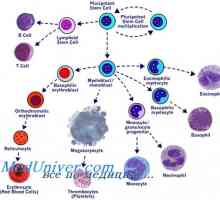 Трансплантация на стволови клетки в миелопролиферативни заболявания mieloleykoze
Трансплантация на стволови клетки в миелопролиферативни заболявания mieloleykoze Трансплантация на стволови клетки в невробластомни тумори и мозъка
Трансплантация на стволови клетки в невробластомни тумори и мозъка Трансплантация на стволови клетки в сърповидно-клетъчна анемия, синдром на Diamond Черно фен
Трансплантация на стволови клетки в сърповидно-клетъчна анемия, синдром на Diamond Черно фен Хематология-остра левкемия (класификация FAB, 1976)
Хематология-остра левкемия (класификация FAB, 1976) Хематология-работна класификация на хематологични злокачествени заболявания
Хематология-работна класификация на хематологични злокачествени заболявания Хематология-трансфузиология (кръвопреливане)
Хематология-трансфузиология (кръвопреливане) Onkologiya-
Onkologiya- Тумори на хемопоеза
Тумори на хемопоеза Заек вирус ще направи трансплантация на костен мозък по-безопасно
Заек вирус ще направи трансплантация на костен мозък по-безопасно Антибиотици се намесват с трансплантация на стволови клетки
Антибиотици се намесват с трансплантация на стволови клетки Програмиране кръвни стволови клетки ще помогне за намаляване на необходимостта от донор
Програмиране кръвни стволови клетки ще помогне за намаляване на необходимостта от донор Хроничната миелоидна левкемия: симптоми, лечение, етап, диагностика, прогноза, каузи
Хроничната миелоидна левкемия: симптоми, лечение, етап, диагностика, прогноза, каузи